Cell Reports, 10 luglio 2018
Neurone o astrocita? Scoperto il gene che guida le staminali adulte nella scelta del loro destino.
Il gene COUP-TFI controlla che le staminali producano la giusta quantità di nuovi neuroni o astrociti. Un eccesso dei secondi è la conseguenza di processi infiammatori associati a patologie tra cui l’Alzheimer. La scoperta del nostro team guidato dalla prof.ssa Silvia De Marchis
Sara Bonzano 1,2,3, Isabella Crisci 1,2, Anna Podlesny-Drabiniok 4, Chiara Rolando 5, Wojciech Krezel 4, Michèle Studer 3, Silvia De Marchis 1,2
L’esistenza di cellule staminali in alcune regioni del cervello dei mammiferi adulti è un dato ormai assodato, ma resta ancora molto da scoprire sui fattori che ne regolano l’attività in condizioni fisiologiche e nella patologia.
Nello studio pubblicato su Cell Reports, il gruppo di ricerca guidato da Silvia De Marchis (del nostro team di Neurogenesi adulta) e del DBIOS, Dipartimento di Scienze della Vita e Biologia dei Sistemi dell’Università di Torino, in collaborazione con il laboratorio dell’Università di Nizza diretto da Michèle Studer, e con il contributo di ricercatori dell’Università di Strasburgo e di Basilea, ha dimostrato che il gene COUP-TFI, già noto per le sue molteplici funzioni nello sviluppo del cervello, gioca un ruolo fondamentale nel controllo delle staminali adulte.
In particolare, le nostre ricercatrici hanno studiato il ruolo di COUP-TFI nelle staminali dell’ippocampo, una regione chiave in processi cognitivi, come la memoria e l’apprendimento. In questa area del cervello, in parallelo alla produzione di nuovi neuroni (neurogenesi), le staminali originano anche gli astrociti, altre cellule fondamentali del sistema nervoso (astrogliogenesi). Un rapporto specifico tra neurogenesi e astrogliogenesi assicura un corretto funzionamento dell’ippocampo, tuttavia fino ad oggi i meccanismi molecolari che regolano questo equilibrio non erano noti ed è proprio su questo aspetto che si è incentrato lo studio di Sara Bonzano e colleghe.
Attraverso l’utilizzo di modelli transgenici abbiamo eliminato in modo selettivo il gene COUP-TFI nelle staminali dell’ippocampo, senza alterarne la funzione durante lo sviluppo. Il risultato di queste manipolazioni è stato una ridotta neurogenesi accompagnata da un aumento nella produzione di nuovi astrociti. Uno sbilanciamento tra neurogenesi e astrogliogenesi ippocampale (a favore di quest’ultima) è tipico della condizione di “neuroinfiammazione” che può portare a deficit cognitivi ed è spesso associata a diverse patologie cerebrali, come ad esempio la malattia di Alzheimer.
Lo studio ha messo in evidenza come proprio il fattore COUP-TFI risultasse ridotto nelle staminali adulte in presenza di neuroinfiammazione. Inoltre, ripristinando la funzione di COUP-TFI nelle staminali nel cervello infiammato è stato possibile ristabilire il corretto rapporto tra neurogenesi e astrogliogenesi.
«I dati ottenuti dimostrano che COUP-TFI è fondamentale per favorire la genesi di nuovi neuroni dalle staminali ippocampali, limitando un programma di “default” diretto alla produzione di astrociti. Lo studio – conclude la prof.ssa De Marchis - oltre a chiarire un meccanismo biologico alla base della produzione di nuovi neuroni nel cervello adulto, apre interessanti prospettive per il trattamento di disfunzioni cognitive associate alle malattie neurologiche. La strada in questa direzione è ancora lunga, e solo grazie a uno sforzo collaborativo congiunto e con nuove risorse a sostegno della ricerca saremo in grado di percorrerla».
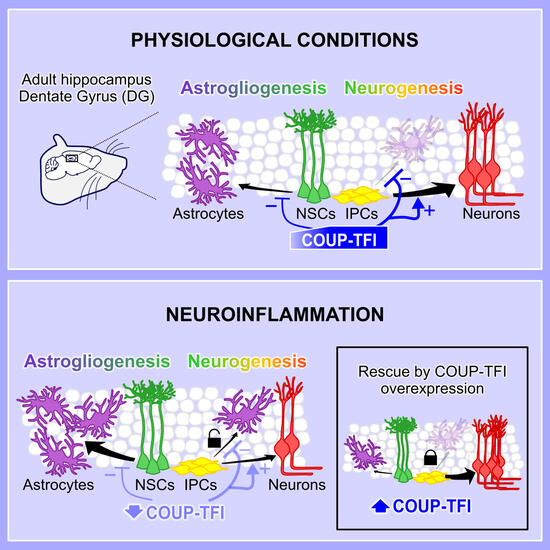
Graphical abstract
Nell'ippocampo del topo adulto, un bilanciamento tra i nuovi neuroni (rossi) e gli astrociti (viola) viene mantenuto in condizioni fisiologiche. Bonzano et al. dimostrano che il fattore di trascrizione COUP-TFI contribuisce a questo equilibrio reprimendo la generazione di nuovi astrociti (freccia con segno -) a favore della neurogenesi (freccia con segno +) nelle staminali/progenitori (verdi/gialli) dell’ippocampo sano e la sua espressione forzata ripristina l'equilibrio tra neurogenesi e astrogliogenesi nell'ippocampo infiammato.
1 Neuroscience Institute Cavalieri Ottolenghi (NICO), University of Turin, Orbassano 10043, Italy;
2 Department of Life Sciences and Systems Biology, University of Turin, Turin 10123, Italy;
3 Université Côte d’Azur (UCA) CNRS, Inserm, iBV, Nice 06108, France;
4 Institut de Génétique et de Biologie Moléculaire et Cellulaire; Inserm, U1258, CNRS, UMR 7104,
Université de Strasbourg France Illkirch 67404;
5 Department of Biomedicine, University of Basel, Basel 4031, Switzerland.
Agenda
Area Ricercatori
Guarda il video
GiovedìScienza racconta la ricerca al NICO
Vivere per sempre.
Una popolazione sempre più longeva, i suoi problemi e le risposte della ricerca
Hai perso la diretta? Guarda ora il video di GiovedìScienza al NICO: una puntata in diretta dai nostri laboratori dedicata alla ricerca sull'invecchiamento.