Brain, maggio 2018
La microdelezione 16p11.2 associata all’autismo altera la connettività funzionale prefrontale (nell’uomo e nel modello murino)
Bertero A1,2, Liska A1, Pagani M1, Parolisi R3, Masferrer ME4, Gritti M5, Pedrazzoli M5, Galbusera A1, Sarica A6, Cerasa A6,7, Buffelli M8, Tonini R5, Buffo A3, Gross C4, Pasqualetti M1,2, Gozzi A1.
Recenti studi sull’uomo hanno dimostrato che diverse varianti genetiche aumentano il rischio di disturbi durante lo sviluppo del sistema nervoso. Tuttavia, non è chiaro come queste varianti possano influire sulla funzione cerebrale e contribuire al rischio neuropsichiatrico.
In questo lavoro, frutto di una collaborazione con diversi Istituti di ricerca, il gruppo guidato da Annalisa Buffo ha studiato una delle più frequenti varianti associate all’autismo, la microdelezione del cromosoma 16p11.2. Dai dati della risonanza magnetica funzionale è emerso che i portatori della microdelezione 16p11.2 presentano una connettività prefrontale compromessa, associata ad alterazioni delle funzioni socio-cognitive. Per confermare questi dati sull’uomo, abbiamo studiato il modello murino con la delezione 16p11.2 che mostra anch’esso una connettività prefrontale alterata. Inoltre, mediante l’analisi ultrastrutturale, abbiamo evidenziato un aumento del diametro assonale nelle fibre callosali che potrebbe rappresentare il correlato cellulare di queste alterazioni.
Questi risultati suggeriscono che la microdelezione 16p11.2 può predisporre a disordini dello sviluppo del sistema nervoso associati a disabilità cognitive attraverso una disregolazione della connettività prefrontale.
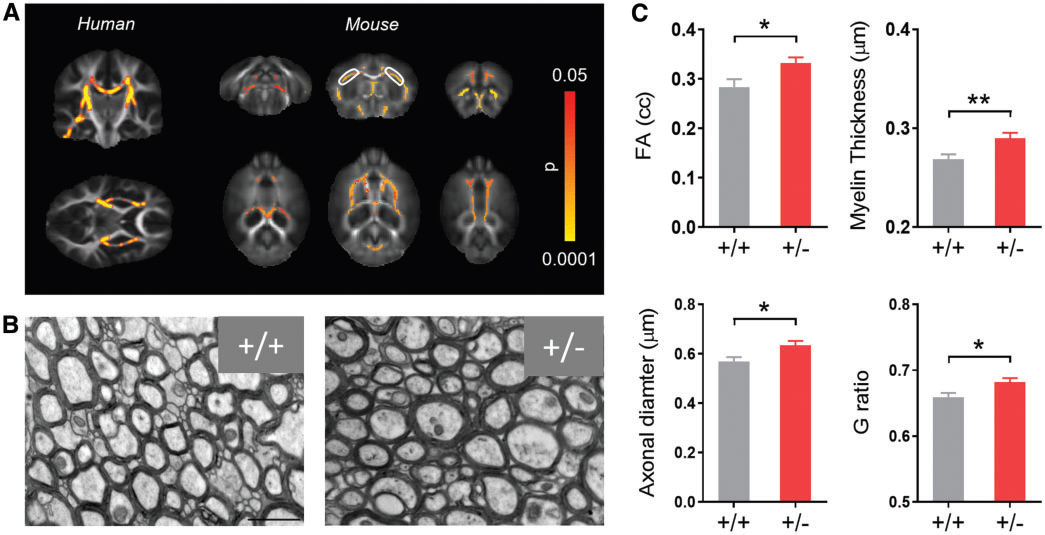
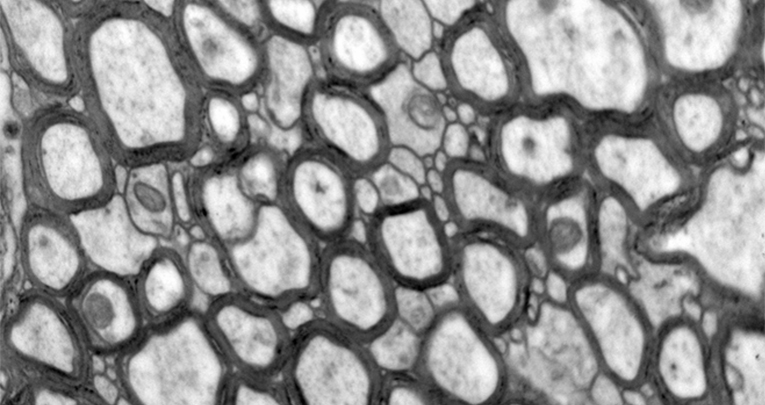
Confronto delle anomalie della sostanza bianca in portatori di delezione 16p11.2 e topi 16p11.2 +/-.
(A) La struttura della sostanza bianca in determinate regioni (colorate in figura) mostra una connettività significativamente maggiore nei portatori di delezione umana (a sinistra, modificata da Owen et al., 2014). L'analisi nel topo ha rivelato analoghi aumenti nei mutanti 16p11.2 + / - (a destra). (B) Immagini rappresentative dell’analisi ultrastrutturale del corpo calloso nei controlli (+/+) e nei topi 16p11.2 +/- (+/-). Scale bar = 1 mm; ingrandimento originale 25 000. (C) Quantificazione dell'anisotropia frazionaria (indicatore dell’organizzazione della struttura della sostanza bianca), dello spessore medio, del diametro assonale e del G-ratio dei neuroni del corpo calloso (* P<0.05, ** P<0.01, media ± SEM).
1 Functional Neuroimaging Laboratory, Istituto Italiano di Tecnologia, Center for Neuroscience and Cognitive Systems @UniTn, Rovereto, Italy.
2 Department of Biology, Unit of Cell and Developmental Biology, University of Pisa, Pisa, Italy.
3 Department of Neuroscience Rita Levi-Montalcini- University of Torino, Neuroscience Institute Cavalieri Ottolenghi (NICO), Torino, Italy.
4 Epigenetics and Neurobiology Unit, European Molecular Biology Laboratory (EMBL), Monterotondo, Italy.
5 Neuroscience and Brain Technologies Department, Istituto Italiano di Tecnologia, Genova, Italy.
6 Consiglio Nazionale delle Ricerche, Catanzaro, Italy.
7 S. Anna Institute and Research in Advanced Neuro-rehabilitation (RAN) Crotone, Italy.
8 Department of Neurosciences, Biomedicine and Movement Sciences, University of Verona, Italy.
Agenda
Area Ricercatori
Guarda il video
GiovedìScienza racconta la ricerca al NICO
Vivere per sempre.
Una popolazione sempre più longeva, i suoi problemi e le risposte della ricerca
Hai perso la diretta? Guarda ora il video di GiovedìScienza al NICO: una puntata in diretta dai nostri laboratori dedicata alla ricerca sull'invecchiamento.