Plos Biology, 27 settembre 2018
Come nasce una stella: origine e sviluppo degli astrociti, le vere 'star' del cervello
Svelato per la prima volta il processo che genera diversi tipi di astrociti nel cervello. Lo studio del nostro gruppo di ricerca guidato da Annalisa Buffo conferma il ruolo cruciale degli astrociti nel corretto sviluppo e mantenimento della funzionalità neuronale, e apre nuove strade per comprendere i disturbi del neurosviluppo.
Valentina Cerrato1,2,*, Elena Parmigiani1,¤,*, Maria Figueres-Oñate3, Marion Betizeau4, Jessica Aprato1, Ishira Nanavaty1, Paola Berchialla5, Federico Luzzati6,2, Claudio de’Sperati7,8, Laura Lopez-Mascaraque3, Annalisa Buffo1,2
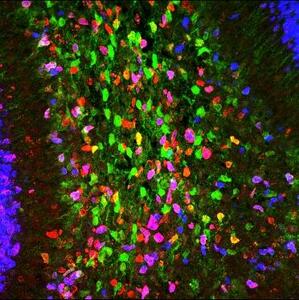
Negli ultimi decenni la classica visione neurone-centrica delle funzioni e disfunzioni cerebrali è stata messa a dura prova: gli astrociti, così denominati per la loro tipica (ma non unica) morfologia stellata, hanno rubato la scena ai neuroni. Queste cellule, a lungo ignorate per il loro presunto ruolo passivo di “collante” tra neuroni, sono in realtà essenziali per il corretto sviluppo, sostegno e modulazione dell’attività neuronale, e il loro coinvolgimento nell’insorgenza di diverse patologie del sistema nervoso è stato più volte dimostrato.
Sulla base della loro eccezionale varietà in termini di morfologia, profili molecolari e specifiche funzioni, gli astrociti possono essere suddivisi in diverse categorie che riflettono, con ogni probabilità, le loro interazioni specializzate con determinate categorie di neuroni. Tuttavia, mentre sull’origine della diversità neuronale le conoscenze sono abbastanza approfondite, rimane ancora da chiarire del tutto come l’eterogeneità degli astrociti sia generata durante lo sviluppo del sistema nervoso.
Nello studio pubblicato sulla prestigiosa rivista Plos Biology, il nostro gruppo di ricerca di Fiosiopatologia delle cellule staminali cerebrali, guidato dalla prof.ssa Annalisa Buffo, ha svelato per la prima volta i meccanismi attraverso i quali i diversi tipi di astrociti sono generati nel cervelletto, un territorio coinvolto nel controllo del movimento che contiene 3 tipi di astrociti ben conosciuti.
Lo studio è frutto di una collaborazione internazionale che, con il coordinamento della prof.ssa Buffo, ha riunito ricercatrici e ricercatori italiani, dell’Università di Torino e dell’IRCCS San Raffaele di Milano, spagnoli (Cajal Institute di Madrid) e svizzeri (Brain Research Institute - Università di Zurigo).
«I risultati del nostro studio - spiega la prof.ssa Buffo - oltre a svelare come l’eterogeneità degli astrociti venga generata durante lo sviluppo, rivelano l’impareggiabile raffinatezza e ripetibilità dei processi biologici alla base della vita. D’altro canto - continua - una così fine regolazione della generazione della diversità degli astrociti non può che confermarne il ruolo cruciale nel corretto sviluppo e mantenimento della funzionalità neuronale, incoronando queste cellule come vere “Star” del cervello, di nome e di fatto».
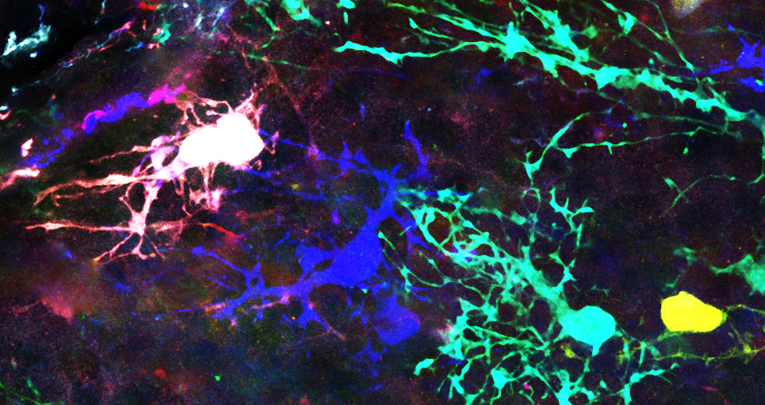
«Mediante analisi clonali di ultima generazione, che permettono di svelare legami di parentela tra cellule sulla base dell’espressione di diverse combinazioni di colori, abbiamo seguito, nel topo, singoli progenitori embrionali e postnatali di astrociti e le loro progenie. Queste analisi – spiega Valentina Cerrato, una delle nostre ricercatrici responsabili dello studio - accoppiate a studi di proliferazione e a simulazioni computerizzate dei diversi lignaggi, hanno permesso di svelare non solo un’inedita multipotenza dei progenitori, in grado di generare uno o più tipi di astrociti, ma anche che l’eterogeneità degli astrociti nel cervelletto deriva da un programma altamente stereotipato e regolato nel tempo e nello spazio».
Secondo un preciso schema costruttivo, infatti, progenie generate in diverse fasi dello sviluppo embrionale occupano territori cerebellari distinti e sono caratterizzate da eterogeneità e capacità di amplificazione che diminuiscono nel tempo. Inoltre, dopo la nascita, diversi ritmi di proliferazione e differenziamento dei vari tipi di astrociti cerebellari risultano in cloni con architetture stereotipate e modularità ricorrenti, basate su rapporti numerici altamente conservati tra tipi di astrociti e, in particolare, nella costante prevalenza di un tipo sugli altri. Questa sorprendente regolarità viene rispettata anche nei sottocloni, gruppi di cellule sorelle separate nello spazio, nei quali i cloni più eterogenei si suddividono.
«Questo studio - commenta la prof.ssa Buffo - oltre ad aprire all’indagine dei meccanismi molecolari che partecipano nella generazione di queste progenie cellulari, offre una nuova chiave di lettura per la comprensione dei disturbi del neurosviluppo, nei quali gli schemi costruttivi astrogliali potrebbero essere alterati con conseguenti anomalie dell’attività neuronale».
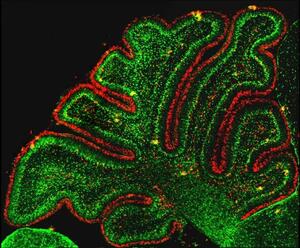
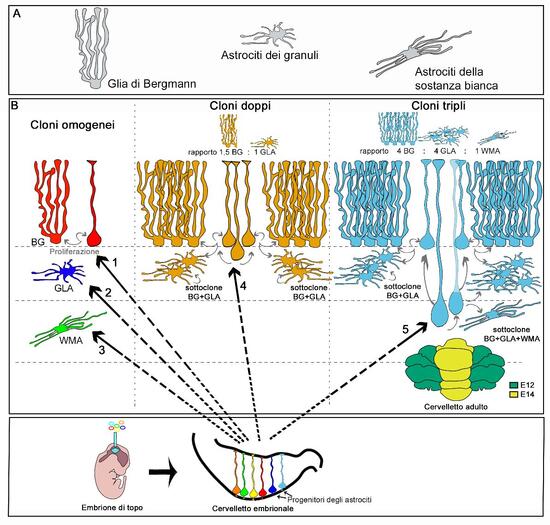
(A) Il cervelletto possiede 3 tipi principali di astrociti: la glia di Bergmann (BG), gli astrociti dei granuli (GLA) e gli astrociti della sostanza bianca (WMA), riconoscibili per forme e caratteristiche funzionali diverse.
(B) L’analisi clonale di ultima generazione “StarTrack” ha consentito di marcare, a partire dall’embrione, singoli progenitori degli astrociti cerebellari con combinazioni di colori differenti, trasmissibili all’intera progenie: nel topo adulto, cellule sorelle sono identificate dalla stessa combinazione di colori. Il nostro studio studio ha svelato che
i) gli astrociti generati in tempi diversi occupano territori cerebellari ben distinti, dai più laterali (colorati in verde nel disegno del cervelletto adulto e popolati dagli astrociti nati al giorno embrionale 12) ai più mediali (in giallo, nei quali si posizionano le cellule nate due giorni dopo);
ii) i progenitori degli astrociti sono multipotenti, ovvero alcuni sono capaci di generare cloni omogenei formati da un solo tipo di astrocita (frecce 1,2,3) mentre altri producono cloni eterogenei comprendenti due o tre sottotipi di cellule diversi (frecce 4 e 5, rispettivamente);
iii) i cloni eterogenei posseggono architetture altamente stereotipate, con rapporti numerici altamente conservati tra tipi di astrociti diversi, rispettati anche a livello dei sottocloni nei quali i cloni più grandi si suddividono.
Plos Biology, September 27, 2018
Multiple origins and modularity in the spatiotemporal emergence of cerebellar astrocyte heterogeneity
Valentina Cerrato1,2,*, Elena Parmigiani1,¤,*, Maria Figueres-Oñate3, Marion Betizeau4, Jessica Aprato1, Ishira Nanavaty1, Paola Berchialla5, Federico Luzzati6,2, Claudio de’Sperati7,8, Laura Lopez-Mascaraque3, Annalisa Buffo1,2
1 Department of Neuroscience Rita Levi-Montalcini, University of Turin, Turin, Italy
2 Neuroscience Institute Cavalieri Ottolenghi, Orbassano, Turin, Italy
3 Department of Molecular, Cellular, and Developmental Neurobiology, Cajal Institute -CSIC-, Spanish National Research Council, Madrid, Spain
4 Brain Research Institute, University of Zurich Irchel, Zurich, Switzerland
5 Department of Clinical and Biological Sciences, University of Turin, Turin, Italy
6 Department of Life Sciences and System Biology, University of Turin, Turin, Italy
7 Laboratory of Action, Perception and Cognition, Vita-Salute San Raffaele University, Milan, Italy
8 Experimental Psychology Unit, Division of Neuroscience, IRCCS San Raffaele Scientific Institute, Milan, Italy
¤ Current address: Department of Biomedicine, University of Basel, Mattenstrasse 28, Basel, Switzerland
* co-first authors
Agenda
Area Ricercatori
Guarda il video
GiovedìScienza racconta la ricerca al NICO
Vivere per sempre.
Una popolazione sempre più longeva, i suoi problemi e le risposte della ricerca
Hai perso la diretta? Guarda ora il video di GiovedìScienza al NICO: una puntata in diretta dai nostri laboratori dedicata alla ricerca sull'invecchiamento.